 |
|
Популярные авторы:: Картленд Барбара :: БСЭ :: Твен Марк :: Громов Дмитрий :: Желязны Роджер :: Лесков Николай Семёнович :: СССР Внутренний Предиктор :: Андреев Леонид Николаевич :: Горький Максим :: Ламур Луис Популярные книги:: Справочник по реестру Windows XP :: Бурый волк :: Течет река Волга… :: Мясоеды :: Необыкновенное приключение некоего Ганса Пфааля :: Информационный листок украинской фантастики N 17-2003 (157) :: Похититель талантов :: Агент галактики :: Тюли-люли :: Нежеланная невеста |
Большая Советская Энциклопедия (МЕ)ModernLib.Net / Энциклопедии / БСЭ / Большая Советская Энциклопедия (МЕ) - Чтение (стр. 67)
рис. 1
). Обнаруженные в 50-60-х гг. 20 в. в юго-западной части Малой Азии следы выплавки меди датируются 7-6-м тыс. до н. э. Примерно в это же время человек познакомился с самородными металлами: золотом, серебром, медью, а затем и с метеоритным железом. Сначала металлические изделия изготовляли путём обработки металлов в холодном состоянии. Медь и железо с трудом подвергались такой обработке и поэтому не могли найти широкого применения. После изобретения горячей кузнечной обработки (ковки) медные изделия получили более широкое распространение (эпоха
)
.Овладение искусством выплавки меди из окисленных медных руд и придания ей нужной формы литьём (5-4 тыс. до н. э.) привело к быстрому росту производства меди и к значительному расширению её применения. Однако ограниченное количество месторождений окисленных медных руд обусловило необходимость освоения гораздо более сложного процесса переработки сульфидных руд с применением предварительного обжига руды и рафинирования меди путём повторного плавления. Возникновение этого процесса относится примерно к середине 2-го тыс. до н. э. (Ближний Восток, Центральная Европа).
Во 2-м тыс. до н. э. начали широко применяться изделия из бронзы (сплава меди с оловом), которые по качеству значительно превосходили медные. Бронзовые орудия труда, оружие и др. предметы отличались большей устойчивостью против коррозии, упругостью, твёрдостью, остротой лезвия. Кроме того, бронза имела более низкую температуру плавления, чем медь, и лучше заполняла литейную форму. Из неё легче было отливать всевозможные изделия. Вытеснение меди бронзой означало переход к .В конце 3-го и во 2-м тыс. до н. э. крупным центром М. меди и бронзы на территории СССР был Кавказ. Примерно в середине 2-го тыс. до н. э. человек начинает овладевать и искусством получения железа из руд. Сначала для этой цели использовали костры, а затем специальные плавильные ямы - сыродутные горны (см. ) .В горн, выложенный из камня, загружали легковосстановимую руду и древесный уголь. Дутьё, необходимое для горения угля, подавалось в горн снизу (первое время естественной тягой, а впоследствии при помощи мехов). Образующиеся газы (окись углерода) восстанавливали окислы железа. Относительно низкая температура процесса и большое количество железистого шлака препятствовали науглероживанию металла и позволяли получать железо только с низким содержанием углерода. Процесс был малопроизводительным и обеспечивал извлечение из руды лишь около половины содержащегося в ней железа. М. железа развивалась очень медленно, несмотря на то, что железные руды гораздо более распространены, чем медные, а температура их восстановления ниже. Причина первоочередного развития М. меди заключается в том, что сыродутное железо по качеству значительно уступало меди. Это объясняется прежде всего тем, что при достижимых в то время температурах процесса медь получалась в расплавленном состоянии, а железо - в виде тестообразной массы с многочисленными включениями шлака и несгоревшего древесного угля. В связи с низким содержанием углерода сыродутное железо было мягким - изготовленные из него оружие и орудия труда быстро затуплялись, гнулись, не подвергались закалке; они уступали по качеству бронзовым. Для перехода к более широкому производству и применению железа необходимо было усовершенствовать примитивный сыродутный процесс, а главное - овладеть процессами науглероживания железа и его последующей закалки, т. с. получения стали. Эти усовершенствования обеспечили железу в 1-м тыс. до н. э. главенствующее положение среди материалов, используемых человеком (см. ) .К началу н. э. М. железа была почти повсеместно распространена в Европе и Азии. На протяжении почти 3 тысячелетий М. железа не претерпела принципиальных изменений. Постепенно процесс совершенствовался: увеличивались размеры сыродутных горнов, улучшалась их форма, повышалась мощность дутья; в результате горны превратились в небольшие печи для производства сыродутного железа - домницы ( рис. 2 ). Дальнейшее увеличение размеров домниц привело в середине 14 в. к появлению небольших доменных печей (см. ) .Увеличение высоты этих печей и более интенсивная подача дутья способствовали повышению температуры и значительно более сильному развитию процессов восстановления и науглероживания металла. Вместо тестообразной массы сыродутного железа в доменных печах получали уже высокоуглеродистый железный расплав с примесями кремния и марганца - чугун. Росту производства чугуна способствовало изобретение в 14 в. способа передела его в ковкое железо - т. н. .Переплавляя чугун в кричном горне, его рафинировали от примесей путём окисления их кислородом дутья и специально загружаемого в горн железистого шлака. Кричный процесс постепенно вытеснил прежние малопроизводительные способы получения стали на основе сыродутного железа, несмотря на достигнутое с их помощью чрезвычайно высокое качество металла (см. , ) .Т. о., возник двухстадийный способ получения железа, сохранивший своё значение и являющийся основой современных схем производства стали. Следующим этапом развития М. стали в Европе было появление в Англии в 1740 (задолго до того известной на Востоке) и в последней четверти 18 в. - .Тигельный процесс был первым способом производства .Её выплавляли в тиглях из огнеупорной глины, которые устанавливались в специальной печи. В пудлинговом процессе, как и в кричном, получали т. н. сварочное железо. Для этого чугун рафинировали от углерода и др. примесей на поду отражательной печи. Несмотря на большое значение для развития техники своего времени, тигельный и пудлинговый процессы не могли удовлетворить потребности в стали. М. чугуна развивалась опережающими темпами. Этому способствовало внедрение водяных воздуходувных труб ( рис. 3 ), мехов с приводом от водяного колеса (с 15 в.), паровых воздуходувных машин (1782). В конце 18 в. в доменном производстве начали широко использовать каменноугольный кокс (1735); к 19 в. относится начало применения нагретого дутья и тщательной подготовки руды к доменной плавке. Отставание сталеплавильного производства проявлялось в том, что количество выплавляемого чугуна долгое время (до начала 20 в.) превышало количество производимой стали. Главная роль в наступившем переломе сыграло изобретение трёх новых процессов производства литой стали: в 1856 - ,в 1864 - мартеновского (см. ) и в 1878 - .Распространение этих процессов (в первую очередь мартеновского, которому свойственно использование большого количества металлического лома) привело к тому, что к середине 20 в. выпуск чугуна составлял уже только 70% от выплавки стали. Дальнейшее развитие сталеплавильного производства во 2-й половине 20 в. связано с существенным увеличением ёмкости и производительности агрегатов, широким применением кислорода для повышения эффективности металлургических процессов, появлением нового, быстро развивающегося способа получения стали в кислородных конвертерах (см. ), с развитием внепечного рафинирования жидкой стали в вакууме, обработки стали синтетическими шлаками и инертным газом, с внедрением , широкой механизацией и автоматизацией производственных процессов. Большое значение в современной М. железа имеет выплавка высококачественной и в том числе , которая с начала 20 в. производится в основном в электропечах (см. ). Со 2-й половины 20 в. для получения некоторых цветных металлов, а также стали особо ответственные назначения начали применять дополнительный переплав металла в , электрошлаковых, электроннолучевых и плазменных установках (см. , , ). В области извлечения железа из руд наряду с доменным производством, которое продолжает расширяться, развиваются разнообразные способы . Этим процессам, позволяющим получать железо, пригодное для выплавки стали в электропечах, принадлежит большое будущее. Кроме железа, в древнем мире добывали и применяли золото, серебро, медь, олово, свинец, ртуть. Многие др. металлы (в т. ч. неизвестные древним) использовались в сплавах, минералах или соединениях. Золото в виде песка и самородков добывали в доисторические времена из россыпей путём промывки. Для получения изделий золотой песок подвергали горячей ковке (кузнечной сварке) или переплавляли в тиглях. При этом обычно получали сплавы золота с серебром и др. элементами, что обусловливало разнообразные вариации цвета, а также литейных и механических свойств металла. золота и отделение его от серебра началось во 2-й половине 2-го тыс. до н. э., но до 6 в. до н. э. распространялось довольно медленно. Удаление примесей (вместе со свинцом, добавляемым для улучшения процесса) производили путём окисления их воздухом. Отделение серебра осуществляли путём хлорирования сплава при нагреве в присутствии поваренной соли, с последующей отгонкой летучих хлоридов или их растворением. Др. способ отделения серебра заключался в переводе его в сульфиды при нагревании сплава с сернистыми материалами и древесным углём. Применение азотной кислоты для отделения серебра от золота относится уже к 13-14 вв. Процесс также был известен в древнем мире, но уверенности в том, что он применялся для извлечения золота из руд и песков, нет. После открытия русским учёным П. Р. в 1843 основ золотых руд и особенно после работ английских металлургов Дж. С. Мак-Артура и бр. Р. и У. Форрестов (1887-88) этот процесс занял ведущее место в М. золота; иногда он используется в соединении с амальгамацией. Успешно применяется для извлечения золота флотационное (см. ) и . Серебро в древности получали главным образом попутно со свинцом из галенита. Начало их совместной выплавки можно отнести к 3-му тыс. до н. э. (Малая Азия); широкое распространение процесс получил только через 1500-2000 лет. Можно полагать, что технологическая схема включала в себя обжиг руды, горновую плавку, разделительную плавку (ликвационное рафинирование, ) и . Во 2-й половине 20 в. свинец получают преимущественно из полиметаллических руд в результате флотационного обогащения, агломерирующего обжига, восстановительной плавки в шахтных печах и рафинирования продукта этой плавки - чернового свинца ( ). При рафинировании извлекается также серебро (и золото, если оно есть). Массовое производство меди началось после изобретения В. А. в 1866 штейна. Большую роль в развитии конвертерной переработки штейна сыграла предложенная в 1880 продувка расплава сбоку (а не снизу, как в бессемеровском способе получения стали из чугуна). При боковой продувке воздух поступает непосредственно в рафинируемый расплав, минуя легко затвердевающую медь, которая собирается на дне конвертера. Огромное значение для массового производства меди имело изобретённое на рубеже 20 в. флотационное обогащение, позволившее успешно перерабатывать руды с содержанием меди менее 1%. Нефлотирующиеся бедные окисленные руды (менее 0,7% Cu) обрабатывают гидрометаллургическим способом (путём ). Сульфидные руды можно выщелачивать в самом месторождении (без добычи руды), используя способ интенсификации выщелачивания с применением бактерий (см. ). Олово в древности выплавляли в простейших шахтных печах, а затем очищали от посторонних примесей посредством ликвационных и окислительных процессов. Коренные оловянные руды перед плавкой подвергали дроблению и простейшему обогащению; из россыпей руду добывали промывкой. В современной М. в связи с необходимостью использования бедных оловянных руд со значительным содержанием примесей (сера, мышьяк, сурьма, висмут, серебро и др.) олово получают по сложным схемам комплексной переработки руд, которые включают в себя обогащение, обжиг, выщелачивание примесей из рудных концентратов, магнитную сепарацию их, восстановительную плавку в отражательных, шахтных или электрических (лучший способ) печах с получением чернового олова и рафинирование его главным образом пирометаллургическим (иногда электролитическим) методом. Первые способы производства ртути сводились, по-видимому, к обжигу руды в кучах; ртуть конденсировалась при этом на холодных предметах. Позднее появилась керамического реторта. Методы получения ртути, описанные немецким учёным Г. (16 в.), сводятся к обжигу руды в керамических сосудах с различными конденсаторами. Железные реторты появились в 17 в. (1641). Затем по мере роста спроса на ртуть получили применение более производительных шахтные печи (периодического, а позднее и непрерывного действия), отражательные печи (с 1842), трубчатые вращающиеся печи (с начала 20 в.), которые служат основным агрегатом для переработки ртутных руд. Перспективный способ получения ртути - переработка руд в , успешно освоенная в СССР. Технологические схемы процессов получения остальных металлов, производство которых достигло значительного уровня только в течение последних столетий (а иногда и лет), освещаются в соответствующих статьях (см. , , , , , и др.). Современная М. как совокупность основных технологических операций производства металлов и сплавов включает в себя: 1) подготовку руд к извлечению металлов (в т. ч. обогащение); 2) процессы извлечения и рафинирования металлов: пирометаллургические, гидрометаллургические, электролитические; 3) процессы получения изделий из металлических порошков путём спекания; 4) кристаллофизические методы рафинирования металлов и сплавов; 5) процессы разливки металлов и сплавов (с получением слитков или отливок); 6) обработку металлов давлением; 7) термическую, термомеханическую, химико-термическую и др. виды обработки металлов для придания им соответствующих свойств; 8) процессы нанесения защитных покрытий. С М. тесно связаны , производство и ряд др. отраслей промышленности. Подготовка руд к извлечению металлов начинается с , , и классификации (см. ). Следующая стадия обработки - обогащение (см. ). В процессе обогащения или после него материалы подвергают обычно или сушке. Весьма перспективен обжиг в кипящем слое. Наибольшее применение в обогатительной технике имеют флотационные, гравитационные, магнитные и электрические методы. Флотационными процессами перерабатывают более 90% всех обогащаемых руд цветных и редких металлов. Из гравитационных процессов распространены обогащение в тяжёлых средах, отсадка, концентрация на столах и др. методы. Большое значение обогатительных процессов в современной М. обусловлено стремлением к повышению эффективности металлургического производства, а также тем, что по мере роста выплавки металлов приходится использовать всё более бедные руды. Непосредственная металлургическая переработка таких руд (без обогащения), как правило, неэкономична, а в некоторых случаях даже невозможна. Заключительными операциями подготовки руд являются обычно их усреднение, смешение, а также посредством , (окомкования) или . Необходимость окускования обусловлена тем, что в процессе обогащения руды подвергаются измельчению, а применение в плавке мелко измельченных материалов в некоторых металлургических производствах нежелательно или недопустимо. Пирометаллургические (высокотемпературные) методы извлечения и рафинирования металлов весьма многообразны (см. ). Они осуществляются в шахтных, отражательных или электрических печах, конвертерах и др. агрегатах. В пирометаллургических процессах происходит концентрирование металлов и удаляемых примесей в различных фазах системы, образующейся при нагреве или расплавлении перерабатываемых материалов. Такими фазами могут служить газ, жидкие металлы, шлак, штейн и твёрдые вещества. После разделения одна или несколько из этих фаз направляются на дальнейшую переработку. Для осуществления необходимых операций в пирометаллургии применяют окислительные, восстановительные и др. процессы. С целью интенсификации окисления успешно используют газообразный кислород, а также хлор и селитру. В качестве восстановителей применяют углерод, окись углерода, водород или некоторые металлы (см. ). Примерами восстановительных процессов могут служить доменная плавка, выплавка вторичной меди, олова и свинца в шахтных печах, получение ферросплавов и титанового шлака в рудовосстановительных электропечах. Магнийтермическим восстановлением получают, например, титан. Окислительное рафинирование является необходимым элементом в мартеновском и конвертерном производстве стали, при получении анодной меди, а также свинца. Весьма широко используются методы извлечения и рафинирования металлов, основанные на образовании сульфидов, хлоридов, иодидов (см. ), карбонилов. Большое значение имеют процессы, базирующиеся на явлениях испарения и конденсации ( , , вакуумная сепарация, ). Получили развитие внепечные методы рафинирования стали, а также и плавка в аргоне, находящие применение при производстве химически активных металлов (титана, циркония, молибдена и др.) и стали. Гидрометаллургические методы извлечения и рафинирования металлов, не требующие высоких температур, базируются на использовании водных растворов (см. ). Чтобы перевести металлы в раствор, применяют выщелачивание с помощью водных растворов кислот, оснований или солей. Для выделения элементов из раствора используют , , , осаждение (см. ) или . Широкое распространение получили металлов ионообменными веществами (в основном синтетическими смолами) и (с помощью органических жидкостей). Современные сорбционные и экстракционные процессы характеризуются высокой эффективностью. Они позволяют извлекать металлы не только из растворов, но и из пульпы, минуя операции отстаивания, промывки и фильтрации. Из др. гидрометаллургических процессов следует отметить автоклавную переработку материалов при повышенных температурах и давлениях (см. ), а также очистку растворов от примесей в кипящем слое. В некоторых производствах применяют извлечение металлов (например, золота) из руд с помощью ртути - амальгамацию. Большое значение в М. имеет получение или рафинирование цветных металлов электролитическим осаждением (см. ) как из водных растворов (медь, никель, кобальт, цинк), так и из расплавов (алюминий, магний). Алюминий, например, получают электролизом криолитглинозёмного расплава. Находит применение также производство изделий из металлических порошков, или . В ряде случаев этот процесс обеспечивает более высокое качество изделий и лучшие технико-экономические показатели производства, чем традиционные способы. Для получения особо чистых металлов и полупроводников применяются кристаллофизические методы рафинирования ( , вытягивание монокристаллов из расплава), основанные на различии составов твёрдой и жидкой фаз при кристаллизации металла из расплава. Процессы получения отливок из расплавленных металлов и сплавов (см. ) и слитков, предназначенных для последующей обработки давлением (см. ), известны человечеству на протяжении многих веков. Основные направления технического прогресса в этой области связаны с переходом к непрерывной разливке стали и сплавов и к совмещенным процессам литья и обработки заготовок давлением (например, бесслитковое получение проволоки или листа из расплавленного алюминия, меди, цинка). Обработка металлов давлением также известна людям очень давно (ковка железа была, например, необходимым элементом процесса переработки крицы). и являются важнейшими составными частями машиностроения. Прокатка - основной способ обработки металлов и сплавов давлением на современныхы металлургических заводах (см. ). Прокатный стан, впервые предложенный, по-видимому, ещё Леонардо да Винчи (1495), превратился в мощный высокоавтоматизированный агрегат, производительность которого достигает несколько млн. тметалла в год. Наряду с листовым и сортовым металлом с помощью прокатных станов получают трубы, гнутые и периодические профили (см. ), и др. виды изделий. Для изготовления проволоки в современной М. широко применяют . Термическая обработка, обеспечивающая получение наиболее благоприятной структуры металлов и сплавов, также имеет весьма древнее происхождение. Такие процессы, как , , и , были известны и хорошо освоены на практике уже в глубокой древности. Научные основы металлов и сплавов были разработаны Д. К. Черновым (см. ). В современной технике термическая обработка металлов и сплавов, а также др. виды обработки (см. , , ) имеют очень широкое применение. Кроме готовых деталей, которые подвергаются обработке на машиностроительных предприятиях, её проходят многие виды продукции и на металлургических заводах. Это относится, например, к стальным рельсам (объёмная закалка или закалка головки), к толстым листам и арматурной стали (упрочняющая обработка), к тонкому листу из трансформаторной стали (отжиг для улучшения магнитных свойств) и т.д. Большое значение в современной М. приобретают процессы нанесения на металл различных защитных покрытий. К таким процессам относятся , , нанесение пластмассовых и др. покрытий, значительно повышающих качество и срок службы металла. Значение М. в создании современной цивилизации исключительно велико. Материальная культура человеческого общества немыслима без металлов; она базируется на них в производстве средств производства, средств транспорта и связи, в строительстве, в военном деле. Большую роль играют металлы в сельском хозяйстве и в производстве предметов потребления. Данные об объёме и динамике производства стали, чугуна, важнейших цветных металлов и др. сведения о М. как отрасли промышленности приведены в статьях , . Лит.:Основы металлургии, т. 1-6, М., 1961-73; Металловедение и термическая обработка стали. Справочник, 2 изд., М., 1961-62; Прокатное производство. Справочник, т. 1-2, М., 1962; Доменное производство. Справочник, т. 1-2, М., 1963; Сталеплавильное производство. Справочник, т. 1-2, М., 1964; Aitchison L., A history of metals, v. 1-2, L., 1960. А. Я. Стомахин. 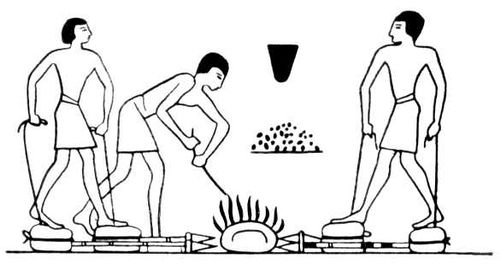
Рис. 1. Плавка металла в Древнем Египте (дутьё подаётся мехами, сшитыми из шкур животных). 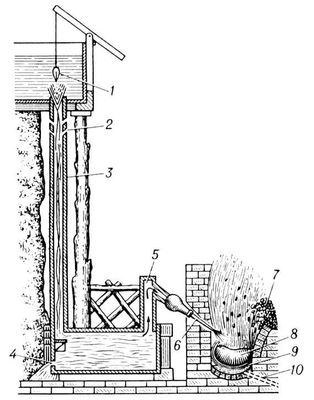
Рис. 3. Каталонский горн с водяной воздуходувной трубой: 1 - клапан; 2 - отверстия для воздуха; 3 - труба; 4 - слив воды; 5 - дутьё; 6 - фурма; 7 - руда и древесный уголь; 8 - крица; 9 - шлак; 10 - выпуск шлака. 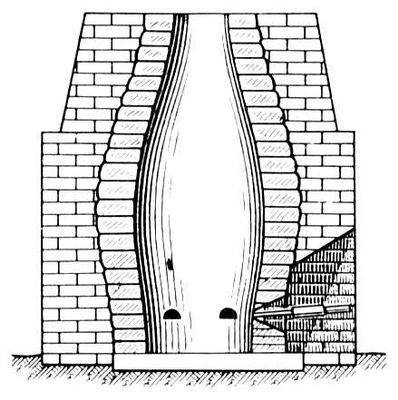
Рис. 2. Домница (штюкофен) в Германии 15-16 вв. Металлы Мета'ллы,простые вещества, обладающие в обычных условиях характерными свойствами: высокой электропроводностью и теплопроводностью, отрицательным температурным коэффициентом электропроводности, способностью хорошо отражать электромагнитные волны (блеск и непрозрачность), пластичностью. М. в твёрдом состоянии имеют кристаллическое строение. В парообразном состоянии М. одноатомны. Перечисленные выше характерные свойства М. обусловлены их электронным строением. Атомы М. легко отдают внешние (валентные) электроны. В кристаллической решётке М. не все электроны связаны со своими атомами. Некоторая их часть (~ 1 на атом) подвижна. Эти электроны могут более или менее свободно перемещаться по М. Существование свободных электронов (электронов проводимости) в М. объясняется зонной теорией (см. ). М. можно представить себе в виде остова из положительных ионов, погруженного в «электронный газ». Последний компенсирует силы электростатического отталкивания между положительными ионами и тем самым связывает их в твёрдое тело (металлическая связь). Из известных (1974) 105 химических элементов 83 - М. и лишь 22 - . Если в длинном или «полудлинном» варианте Менделеева провести прямую линию от бора до астата (табл. 1), то можно считать, что неметаллы расположены на этой линии и справа от неё, а М. - слева. Не следует, однако, абсолютизировать ни свойства, характерные для М., ни их отличия от неметаллов. Металлический блеск присущ только компактным металлическим образцам. Тончайшие листки Ag и Au (толщиной 10 -4 мм) просвечивают голубовато-зелёным цветом. Мельчайшие порошки М. часто имеют чёрный или черно-серый цвет. Некоторые металлы (Zn, Sb, Bi) при комнатной температуре хрупки и становятся пластичными только при нагревании. Вся совокупность перечисленных выше свойств присуща типичным М. (например, Cu, Au, Ag, Fe) при обычных условиях (атмосферном давлении, комнатной температуре). При очень высоких давлениях (~ 10 5-10 6 ам) свойства М. могут существенно измениться, а неметаллы приобрести металлические свойства. Многие простые вещества по одним свойствам можно отнести к М., по др. - к неметаллам. Особенно много такого рода «нарушений» имеет место вблизи границы, проведённой в табл. 1. Так, Ge по внешнему виду - М., в химическом отношении проявляет себя скорее как М. (легче отдаёт электроны, чем принимает), а по величине и характеру электропроводности Ge - полупроводник. Сурьма Sb имеет электросопротивление слишком большое для М., однако температурный коэффициент сопротивления у Sb положительный и большой, как у М.; по способности отдавать электроны Sb также относится к М. As, Sb и Bi иногда называют .Po по внешнему виду - М., в химическом отношении ему присущи свойства и М., и неметалла - наряду с положительной валентностью (точнее окислительным числом) проявляется и отрицательная (- 2). Металлические сплавы по свойствам имеют много общего с М., поэтому в физической, технической и экономической литературе нередко к М. относят также и . Историческая справка.Термин «металл» произошёл от греческого слова mйtallon (от metallйuo - выкапываю, добываю из земли), которое означало первоначально копи, рудники (в этом смысле оно встречается у Геродота, 5 в. до н. э.). То, что добывалось в рудниках, Платон называл metallйia. В древности и в средние века считалось, что существует только 7 М.: золото, серебро, медь, олово, свинец, железо, ртуть (см. ) .По алхимическим представлениям, М. зарождались в земных недрах под влиянием лучей планет и постепенно крайне медленно совершенствовались, превращаясь в серебро и золото (см. ) .Алхимики полагали, что М. - вещества сложные, состоящие из «начала металличности» (ртути) и «начала горючести» (серы). В начале 18 в. получила распространение гипотеза, согласно которой М. состоят из земли и «начала горючести» - флогистона. М. В. Ломоносов насчитывал 6 М. (Au, Ag, Cu, Sn, Fe, Pb) и определял М. как «светлое тело, которое ковать можно». В конце 18 в. А. Л. Лавуазье опроверг гипотезу флогистона и показал, что М. - простые вещества. В 1789 Лавуазье в руководстве по химии дал список простых веществ, в который включил все известные тогда 17 М. (Sb, Ag, As, Bi, Со, Cu, Sn, Fe, Mn, Hg, Mo, Ni, Au, Pt, Pb, W, Zn). По мере развития методов химического исследования число известных М. возрастало. В 1-й половине 19 в. были открыты спутники Pt, получены путём электролиза некоторые щелочные и щёлочноземельные М., положено начало разделению редкоземельных металлов, открыты неизвестные М. при химическом анализе минералов. В 1860-63 методом спектрального анализа были открыты Cs, Rb, Tl, In. Блестяще подтвердилось существование М., предсказанных Д. И. Менделеевым на основе его периодического закона. Открытие в конце 19 в. повлекло за собой поиски природных радиоактивных М., увенчавшиеся полным успехом. Наконец, методом ядерных превращений начиная с середины 20 в. были искусственно получены радиоактивные М., в частности . В конце 19 - начале 20 вв. получила физико-химическую основу металлургия - наука о производстве М. из природного сырья. Тогда же началось исследование свойств М. и их сплавов в зависимости от состава и строения (см. , ) . Химические свойства.В соответствии с местом, занимаемым в периодической системе элементов (табл. 1), различают М. главных и побочных подгрупп. М. главных подгрупп (подгруппы а) называют также непереходными. Эти М. характеризуются тем, что в их атомах происходит последовательное заполнение s- и р-электронных оболочек. В атомах М. побочных подгрупп (подгруппы б), называют переходными, происходит достраивание d- и f-оболочек, в соответствии с чем их делят на d-группу и две f-группы - и .В подгруппы а входят 22 М.: Li, Na, К, Rb, Cs, Fr (I a); Be, Mg, Ca, Sr, Ba, Ra (II a); Al, Ga, In, Tl (III a); Ge, Sn, Pb (IV a); Sb, Bi (V a); Po (VI а). В подгруппы б входят: 1) 33 переходных металла d-группы [Cu, Ag, Au (I б), Zn, Cd, Hg (II б); Sc, Y, La, Ac (III б); Ti, Zr, Hf, Ku (IV б); V, Nb, Ta, элемент с Z = 105 (V б), Cr, Mo, W (VI б), Mn, Te, Re (VII б), Fe, Co, Ni, Ru, Rh, Pd, 0s, lr, Pt (VIII б)]; 2) 28 М. f-группы (14лантаноидов и 14 актиноидов). Электронная структура атомов некоторых d-элементов имеет ту особенность, что один из электронов внешнего уровня переходит на d-подуровень. Это происходит при достройке этого подуровня до 5 или 10 электронов. Поэтому электронная структура валентных подуровней атомов d-элементов, находящихся в одной подгруппе, не всегда одинакова. Например, Cr и Mo (подгруппа VI б) имеют внешнюю электронную структуру соответственно 3d 54s 1и 4d 55s 1, тогда как у W она 5d 46s 2. В атоме Pd (подгруппа VIII б) два внешних электрона «перешли» на соседний валентный подуровень, и для атома Pd наблюдается d 10вместо ожидаемого d 8s 2. 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90 |
|||||||