 |
|
Популярные авторы:: Андерсон Пол Уильям :: БСЭ :: Ламур Луис :: Лесков Николай Семёнович :: Биленкин Дмитрий Александрович :: Ломер Кит :: Картленд Барбара :: Желязны Роджер :: Коллектив Рубоард :: Бондарев Юрий Васильевич Популярные книги:: Справочник по реестру Windows XP :: Согровища негуса :: Бурый волк :: Принц убивший дракона :: Солдат трех армий :: Смерть Эльзы Басколет :: Маленький Архимед :: Зеленый храм :: Властелин Окси-мира :: «Простите нас!» |
Большая Советская Энциклопедия (РА)ModernLib.Net / Энциклопедии / БСЭ / Большая Советская Энциклопедия (РА) - Чтение (стр. 60)
Различение Р. и р. как двух «способностей души» намечается уже в античной философии: если рассудок - способность рассуждения - познаёт всё относительное, земное и конечное, то разум, сущность которого состоит в целеполагании, открывает абсолютное, божественное и бесконечное. У
, Дж.
,
И.
, Ф.
,
Ф
.
и др. сложилось представление о разуме как высшей по сравнению с рассудком способности познания: разум непосредственно «схватывает» единство противоположностей, которые рассудок разводит в стороны. Согласно И.
, основной функцией рассудка в познании является мыслительное упорядочение явлений. Разум же, пользующийся средствами рассудка, стремится постигнуть
, но не достигает этой цели и остаётся в границах рассудка. Г.
истолковывал рассудок как «... необходимый момент разумного мышления» (Соч., т. 3, М., 1956, с. 278). Диалектический метод, по мысли Гегеля, на высшей своей ступени предстаёт как «... рассудочный разум или разумный рассудок» (там же, т. 5, М., 1937, с. 4). Вместе с тем Гегель отождествил рассудок с метафизическим пониманием действительности и противопоставил его диалектике разума. С точки зрения диалектического материализма, процесс развития теоретического мышления предполагает взаимосвязь Р. и р. С рассудком связана способность строго оперировать понятиями, правильно классифицировать факты и явления, приводить знания в определённую систему. Опираясь на рассудок, разум выступает как творческая познавательская деятельность, раскрывающая сущность действительности. Посредством разума мышление синтезирует результаты познания, создаёт новые идеи, выходящие за пределы сложившихся систем знания.
Рассыпное Рассыпно'е,посёлок городского типа в Донецкой области УССР. Подчинён Торезскому горсовету. Ж.-д. станция (Рассыпная) на линии Дебальцево - Иловайское. Добыча угля. Рассыпной строй Рассыпно'й строй,расчленённое по фронту построение подразделений (групп) пехоты в наступлении в конце 18-19 вв. В русской армии Р. с. впервые был применен П. А. Румянцевым и с некоторыми изменениями сохранялся до введения стрелковых цепей в начале 20 в. (см. ). Рас-Таннура Рас-Танну'ра,город на В. Саудовской Аравии. Крупный порт Персидского залива (грузооборот 169,8 млн. тв 1971). Соединён шоссе с портами Даммам и Эль-Хубар, центром нефтеразработок Дахран. Два завода, по переработке нефти (главным образом мазут и дизельное топливо) и по переработке попутного нефтяного газа (производство сжиженного пропана и бутана). Растачивание Раста'чивание,процесс механической обработки внутренних поверхностей расточными с целью увеличения диаметра. Р. осуществляется на токарных, расточных и др. металлорежущих станках. Можно обрабатывать сквозные и глухие цилиндрическими и коническими отверстия, выемки, канавки и др. Точность обработки при Р. - 4-5-го классов, шероховатость поверхности - 2-3-го классов чистоты. Растворимости диаграмма Раствори'мости диагра'мма,графическое изображение равновесного состава растворов в зависимости от температуры, а также от давления и других параметров, характеризующих внешние условия. Р. д. является частным случаем , широко используемых в химической термодинамике. Р. д. двойных жидких систем с ограниченной взаимной растворимостью компонентов Аи В(нитробензола и н-гексана) показана на рис . Каждой точке а'вне заштрихованной области соответствует ненасыщенный раствор одного компонента в другом. Каждая точка на кривой, ограничивающей эту область, представляет насыщенный раствор. Каждой же точке авнутри заштрихованной области отвечает двухфазная система из слоя насыщенного раствора Ав В, состав которого определяется точкой b, и слоя насыщенного раствора Bв A, состав которого определяется точкой с.Выше некоторой температуры Т кр- критической температуры растворимости (растворения) - у многих систем наступает неограниченная взаимная растворимость (см. ). Составы обоих слоев при этой температуре становятся одинаковыми. Если кривая, ограничивающая область расслоения, имеет максимум, то Т крназывается верхней критической температурой растворимости (см. рис. ), если минимум - нижней критической температурой растворимости. Существуют системы (например, вода - никотин), на Р. д. которых имеются обе критические температуры. См. , , . 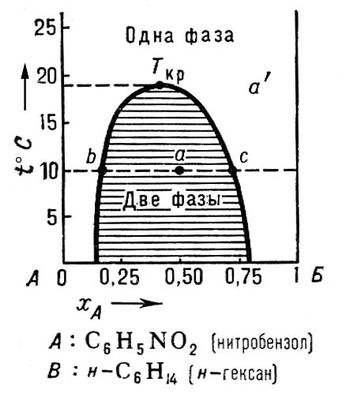
Рис. к ст. Растворимости диаграмма. Растворимость Раствори'мость,способность вещества образовывать с другим веществом однородную, термодинамически устойчивую систему переменного состава, состоящую из двух или большего числа компонентов. Такие системы возникают при взаимодействии газов с жидкостями, жидкостей с жидкостями и т.д. (см. ). Соотношение компонентов может быть либо произвольным, либо ограниченным некоторыми пределами. В последнем случае Р. называют ограниченной. Мерой Р. вещества при данных условиях служит его .Р. различных веществ в определённом зависит от внешних условий, прежде всего - от температуры и давления. Давление наиболее сильно сказывается на Р. газов. Изменение внешних условий влияет на Р. в соответствии с принципом смещения равновесий (см. ). Для наиболее важных растворителей составлены таблицы Р. различных веществ в зависимости от внешних условий или только для стандартных условий. Растворители Раствори'тели,индивидуальные химические соединения или смеси, способные растворять различные вещества, т. е. образовывать с ними однородные системы переменного состава, состоящие из двух или большего числа компонентов (см. ). Для систем жидкость - газ и жидкость - твёрдое вещество Р. принято считать жидкий компонент; для системы жидкость - жидкость - компонент, находящийся в избытке. В принципе любое вещество может быть Р. для какого-либо другого вещества. Однако на практике к Р. относят только такие вещества, которые отвечают определённым требованиям. Например, Р. должны обладать хорошей, т. н. активной растворяющей способностью, быть достаточно химически инертными по отношению к растворяемому веществу и аппаратуре. Р., применяемые в промышленности, должны быть доступными и дешёвыми. В зависимости от отрасли промышленности к Р. предъявляют различные др. требования, обусловленные особенностями производства. Так, для пригодны Р., обладающие избирательной растворяющей способностью, для др. процессов часто применяют т. н. сочетающиеся Р., улучшающие взаимную растворимость, и т.д. Наиболее употребительна химическая классификация, в соответствии с которой все Р. подразделяются на неорганические и органические. Самым распространённым неорганическим Р., применяемым для большого числа неорганических и органических соединений, является .К неорганическим Р. относятся также: жидкий аммиак - хороший Р. для щелочных металлов, фосфора, серы, солей, аминов и др. веществ; жидкий сернистый ангидрид - Р. для многих органических и неорганических соединений, используемый, в частности, в промышленности для очистки нефтепродуктов; расплавленные металлы и соли и т.д. Большое значение имеют многочисленные органические Р. Это прежде всего (в т. ч. углеводороды и их галогенопроизводные), спирты, простые и сложные эфиры, кетоны, нитросоединения. Органические Р. очень широко применяются в производстве пластмасс, лаков и красок, синтетических волокон, смол, клеев в резиновой промышленности, при экстракции растительных жиров, для химической чистки одежды; кроме того, их используют для очистки химических соединений перекристаллизацией, при хроматографическом разделении веществ, для создания определённой среды и т.д. Можно выделить группы Р. в зависимости от др. характеристик: температуры кипения - низкокипящие Р. (например, этиловый спирт, метилацетат) и высококипящие Р. (например, ксилол); относительной скорости испарения - быстроиспаряющиеся и медленноиспаряющиеся (в качестве эталона часто берут скорость испарения бутилацетата); полярности - неполярные (углеводороды, сероуглерод) и полярные (например, вода, спирты, ацетон). Технические условия на Р. обычно содержат данные и по температуре вспышки, по пределам взрывоопасных концентраций паров в воздухе, по давлению пара при стандартных температурах, а также по растворяющей способности - для какого типа веществ можно использовать данный Р. (для растворения масел и жиров, смол, красителей, каучуков натуральных и синтетических и т.п.). В качестве Р. распространены и смеси различных индивидуальных веществ, например бензины, петролейный эфир, смеси спиртов и эфиров. К числу Р. часто относят также ,служащие для улучшения механических и физических свойств каучуков, природных смол, полиамидов и многих других высокомолекулярных соединений. Почти все органические Р. физиологически активны. Некоторые из них - ароматические углеводороды, хлорпроизводные, амины, кетоны - при значительных концентрациях могут вызывать серьёзные отравления, другие приводят к различным кожным заболеваниям (дерматитам). Для многих промышленных органических Р. разработаны технические условия по обеспечению как противопожарной безопасности при работе с ними, так и личной защиты от их физиологически вредных воздействий. Лит.:Справочник химика, 2 изд., т. 6, Л., 1967, с. 118-54; Неводные растворители, пер. с англ., М., 1971. См. также лит. при ст. . Растворители нефтяные Раствори'тели нефтяны'е,индивидуальные жидкие углеводороды или их смеси, получаемые из нефти и применяемые в качестве в промышленных производствах и при лабораторных работах. Р. н. хорошо растворяют все нефтяные фракции, растительные масла и жиры, органические соединения серы, кислорода и азота. Растворяющая способность растворителя возрастает с повышением содержания в нём ароматических углеводородов. Все Р. н. плохо растворяют воду (сотые доли процента). Ароматические растворители плохо растворяют твёрдые парафины, а жидкий пропан - асфальтосмолистые вещества. Р. н. обладают невысокой токсичностью (бензол, толуол и ксилол), огне- и взрывоопасны. Жидкий пропан используется для деасфальтизации гудрона. Пентан, гексан, гептан и октан применяются в лабораторной практике. Бензол, толуол и технический ксилол - растворители, используемые при производстве пластмасс, смол, лаков, красок и мастик. Бензин - растворитель для резиновой промышленности - используется для приготовления резинового клея, специальных (быстросохнущих) масляных лаков, красок. Уайт-спирит применяется в лакокрасочной и олифоварочной промышленности для растворения масляных эмалей, битумного и электроизоляционного лаков. Экстракционный бензин извлекает масла из семян и жмыхов, жир из костей, никотин из махорочного листа. Бензин для промышленно-технических целей применяется в производстве искусственных кож, для химической чистки тканей, промывки деталей при ремонте и смывания противокоррозионных покрытий. Основные показатели Р. н. приведены в таблице. Основные показатели растворителей нефтяных а
аРастворители не должны содержать сероводород, меркаптаны, кислоты, щёлочи, воду и механические примеси. Содержание ароматических углеводородов в петролейном эфире марки 40-70 и 70-100 не должно превышать 3%, в экстракционном бензине - 4% и уайт-спирите - 16%. Нефтяной толуол должен содержать не менее 95% сульфируемых соединений. б10% выкипает не ниже указанной температуры. в95% выкипает не выше указанной температуры. Лит.:Товарные нефтепродукты, их свойства и применение. Справочник, под ред. Н. Г. Пучкова, М., 1971; Нефтепродукты, М., 1970; Папок К. К., Рагозин Н. А., Технический словарь-справочник по топливу и маслам, 3 изд., М., 1963. Растворонасос Растворонасо'с,машина для транспортирования свежеприготовленных штукатурных и кладочных растворов по трубам или шлангам к месту производства работ. Принцип действия Р. основан на засасывании и нагнетании раствора. В зависимости от способа воздействия на подаваемый раствор различают Р. диафрагменные и бездиафрагменные. В СССР применяют Р. производительностью 1-6 м 3/ ч. Р.обеспечивают дальность перемещения растворов до 200 мпо горизонтали и до 40 мпо вертикали. Предельное рабочее давление, создаваемое в Р., - 1-1,5 Мн/ м 2(10-15 кгс/с 2). Растворосмеситель Растворосмеси'тель,машина для приготовления строительных растворов путём смешивания различных компонентов. Различают Р. гравитационные и с принудительным перемешиванием; передвижные производительностью 1,5-5 м/ чи стационарные - до 100 м 3/ ч.В СССР широкое распространение получили Р. периодического действия с принудительным перемешиванием в неподвижном смесительном барабане. Наибольший объём готового замеса отечественного Р. -1800 л. Передвижные Р. со смесительным барабаном ёмкостью 150 ли более снабжены скиповым подъёмником и дозатором воды. Растворы полимеров Раство'ры полиме'ров,термодинамически устойчивые однородные молекулярно-дисперсные смеси полимеров и низкомолекулярных жидкостей. В разбавленных Р. п. макромолекулы отделены друг от друга, и изучение свойств Р. п. (оптических, электрических, гидродинамических) позволяет получить количественную информацию о молекулярной массе и молекулярно-массовом распределении растворённого полимера, размерах, форме и жёсткости макромолекул. Усиление межмолекулярного взаимодействия с повышением концентрации приводит в Р. п. к появлению трёхмерной сетки связей, вплоть до застудневания (см. ), а также к формированию флуктуационных или устойчивых ассоциатов различной формы, которые могут приближаться по своим размерам к коллоидным частицам (см. ). Во многих практических случаях граница между Р. п., студнями и коллоидными системами условна и определение её может зависеть от принятого метода исследования. Растворимость полимеров зависит от химического строения их цепей, природы растворителя и температуры. Вследствие гибкости в Р. п. появляется известная независимость движения отдельных частей молекулы, что отражается на многих измеряемых свойствах Р. п. как кажущееся резкое увеличение числа частиц растворённого компонента по сравнению с его истинным содержанием. Поэтому для Р. п. характерны очень высокие вязкости, сильная зависимость вязкости от концентрации, а также ряд термодинамических аномалий по сравнению с растворами низкомолекулярных соединений. Из-за малой скорости диффузии макромолекул наблюдается очень медленное приближение к равновесному состоянию при смешении и образование Р. п. через стадию полимера. Р. п. обладают вязкоупругими свойствами, а концентрированные растворы, подобно резинам, способны к высокоэластическим деформациям (см. ). Р. п. широко применяют при получении волокон и плёнок, клеев, лаков, красок и др. изделий из полимерных материалов. Введение в полимер малых количеств растворителя ( ) используют в технологии полимеров для снижения температур стеклования и текучести, а также для понижения вязкости расплава. Лит.:Тагер А, А., Физико-химия полимеров, 2 изд., М., 1968, гл. 13-17; Цветков В. Н., Эскин В. Е., Френкель С. Я., Структура макромолекул в растворах, М., 1964; Моравец Г., Макромолекулы в растворах, пер. с англ., М., 1967; Папков С. П., Физико-химические основы производства искусственных и синтетических волокон, М., 1972. А. Я. Малкин. Растворы (строит.) Раство'рыстроительные, строительные материалы, получаемые в результате затвердевания рационально подобранных смесей вяжущего вещества (с водой, реже без неё) и мелкого заполнителя - растворных смесей. (Нередко термин «Р.» неправомерно употребляют в значении «растворная смесь».) В соответствии с назначением Р. их подразделяют на кладочные, применяемые при возведении (преимущественно из кирпича, бутового камня), отделочные - для и нанесения декоративных слоев на стеновые панели и блоки, специальные (гидроизоляционные, кислотоупорные, акустические, тампонажные и др.). По виду вяжущего вещества (см. ) различают Р. на неорганических вяжущих: цементные, известковые, гипсовые и смешанные (например, известково-цементные) и на органических вяжущих: полимеррастворы (см. ), асфальтовые растворы (см. ) и др. В зависимости от объёмной массы Р. делят на тяжёлые (на обычном песке) - объёмной массой 1500-2500 кг/ м 3и лёгкие - объёмной массой менее 1500 кг/ л 3(для получения последних используют мелкие пористые , а также поризацию вяжущего теста). По прочности на сжатие Р. подразделяют на 9 марок - от «4» до «300» (4-300 кгс/ см 2 ,или 0,4-30 Мн/ м 2). Наиболее широко применяются кладочные и отделочные Р. на минеральных вяжущих. Общая теория таких Р. впервые была разработана в СССР в 30-х гг. Н. А. .Будучи аналогичными по составу , Р. отличаются от последних повышенной пластичностью растворной смеси и, обычно, меньшей прочностью, что обусловливает специфику их применения - преимущественно в виде тонких слоев, получаемых укладкой растворной смеси на пористое основание (кирпич, дерево и др.). Для получения Р. требуемой прочности растворная смесь должна обладать необходимой подвижностью и водоудерживающей способностью. Степень подвижности растворной смеси устанавливают по глубине погружения в неё стандартного металлического конуса (т. н. конуса СтройЦНИЛ). Водоудерживающая способность характеризуется свойством растворной смеси не расслаиваться при транспортировке и сохранять влажность при укладке (на пористое основание), необходимую для нормального процесса её твердения. С целью экономии цемента при изготовлении т. н. низкомарочных Р. и для придания растворной смеси повышенной пластичности используют ряд приёмов: добавляют к цементу малопрочные, но высокопластичные вяжущие (известь, глину); вводят в растворную смесь тонкомолотые (шлаки, золы ТЭС, песок и др.), применяют пластифицирующие поверхностно-активные добавки. Приготовляют растворные смеси, как правило, на специализированных заводах или растворосмесительных узлах, откуда они поступают на строительные объекты. Выпускаются также сухие растворные смеси, которые перед употреблением смешивают с водой. На строительной площадке растворные смеси транспортируют к месту производства работ . В современном строительстве получают распространение Р. на смеси полимерного и минерального вяжущих (например, поливинилацетатцементные), обладающие высокой прочностью сцепления с основанием, и Р. на полимерных вяжущих (полимеррастворы), отличающиеся высокими химическими стойкостью, прочностью и декоративными качествами. Такие Р. применяют главным образом для устройства покрытий полов в общественных и промышленных зданиях. Лит.:Строительные нормы и правила, ч. 1, разд. В, гл. 2. Вяжущие материалы неорганические и добавки для бетонов и растворов, М., 1969; Указания по приготовлению и применению строительных растворов, СН 290-64, М., 1965; Воробьев В. А., Комар А. Г., Строительные материалы, М., 1971, К. Н. Попов. Растворы (химич.) Раство'ры,макроскопически однородные смеси двух или большего числа веществ (компонентов), образующие термодинамически равновесные системы. В Р. все компоненты находятся в молекулярно-дисперсном состоянии; они равномерно распределены в виде отдельных атомов, молекул, ионов или в виде групп из сравнительно небольшого числа этих частиц. С термодинамической точки зрения Р. - фазы переменного состава, в которых при данных внешних условиях соотношение компонентов может непрерывно меняться в некоторых пределах. Р. могут быть газообразными, твёрдыми (см. ). Чаще же всего термин «Р.» относят к жидким Р. Практически все жидкости, встречающиеся в природе, представляют собой Р.: морская вода - Р. большого числа неорганических и органических веществ в воде, нефть - Р. многих, как правило органических, компонентов и т.д. Р. широко представлены в технике и повседневной практике человека. Простейшие составные части Р. (компоненты) обычно могут быть выделены в чистом виде; их смешением можно вновь получить Р. любого допустимого состава. Количественное соотношение компонентов определяется их концентрациями. Обычно основной компонент называют растворителем, а остальные компоненты - растворенными веществами. Если одним из компонентов является жидкость, а другим - газы или твёрдые вещества, то растворителем считают жидкость. Классификация Р. основана на различных признаках. Так, в зависимости от концентрации растворённого вещества Р. делят на концентрированные и разбавленные; в зависимости от характера растворителя - на водные и неводные (спиртовые, аммиачные и т.п.); в зависимости от концентрации ионов водорода - на кислые, нейтральные и щелочные. В соответствии с термодинамическими свойствами Р. подразделяют на те или иные классы, прежде всего - на идеальные и неидеальные (называемые также реальными). Идеальными Р. называют такие растворы, для которых m i каждого компонента iимеет простую логарифмическую зависимость от его концентрации (например, от мольной доли x i): m
i
=
где через обозначен химический потенциал чистого компонента, зависящий только от давления ри температуры Т,и где R - .Для идеальных Р. энтальпия смешения компонентов равна нулю, энтропия смешения выражается той же формулой, что и для идеальных газов, а изменение объёма при смешении компонентов равно нулю. Эти три свойства идеального Р. полностью характеризуют его и могут быть взяты в качестве определяющих для идеального Р. Для идеальных Р. выполняются и .Опыт показывает, что Р. идеален только в том случае, если образующие его компоненты сходны друг с другом прежде всего в отношении геометрической конфигурации и размера молекул. Наиболее близки к идеальным Р. смеси соединений с изотопозамещёнными молекулами. Как правило, для идеальных Р. соотношение (1) справедливо во всей области изменения концентраций. Концентрации, при которых в данном Р. начинают обнаруживаться заметные отклонения от идеальности, очень сильно зависят от природы образующих его веществ. Большинство достаточно разбавленных Р. ведут себя как идеальные. Р., не обладающие свойствами идеальных Р., называются неидеальными. Для них выполняется соотношение, аналогичное (1) при замене концентрации на активность: a i= g ix i,где a i- активность компонента i,g i - коэффициент активности, зависящий как от концентрации данного компонента, так и от концентраций остальных компонентов, а также от давления и температуры. Среди неидеальных Р. большой класс составляют регулярные Р., которые характеризуются той же энтропией смешения, что и идеальные Р., однако их энтальпия смешения отлична от нуля и пропорциональна логарифмам коэффициентов активности. Особый класс составляют атермальные Р., у которых теплота смешения равна нулю, а коэффициенты активности определяются только энтропийным членом и не зависят от температуры. Теория таких Р. часто позволяет предсказывать свойства неидеальных Р., например в случае неполярных компонентов с сильно различающимися молекулярными объёмами. Близки к атермальным многие Р. высокомолекулярных соединений в обычных растворителях. При определённых температуре и давлении растворение одного компонента в другом обычно происходит в некоторых пределах изменения концентраций. Р., находящийся в равновесии с одним из чистых компонентов, называемом насыщенным (см. ), а его концентрация - этого компонента. Графически зависимость растворимости от температуры и давления представляется .При концентрациях растворённого вещества, меньших его растворимости, Р. является ненасыщенным. Если Р. не содержит центров , то его можно переохладить так, что концентрация растворённого вещества окажется выше его растворимости, а Р. становится пересыщенным. Ряд практически важных свойств Р. связан с изменением давления насыщенного пара растворителя над Р. при изменении концентрации растворённого вещества: понижение температуры замерзания (см. ), повышение температуры кипения (см. ) и т.д. Строение Р. определяется прежде всего характером компонентов, его образующих. Если компоненты близки по химическому строению, размерам молекул и т.п., то строение Р. принципиально не отличается от строения чистых жидкостей. Молекулы веществ, заметно отличающихся по своему строению и свойствам, обычно сильнее взаимодействуют друг с другом, что приводит к образованию комплексов в Р., которые вызывают отклонения от идеальности. Энергии образования этих комплексов достигают величин нескольких кдж/ моль, что позволяет говорить о существовании в Р. слабых химических взаимодействий и образовании тех или иных химических соединений - новых компонентов Р. Взаимодействие с молекулами растворителя сопровождается у многих веществ (например, электролитов) обратным процессом - .Соли, при растворении в воде и др. полярных растворителях частично или полностью распадаются на ионы, вследствие чего число различных частиц в Р. увеличивается. При электролитической диссоциации суммарная электронейтральность Р. сохраняется; около каждого иона образуется слой более тесно связанных с ним молекул растворителя - сольватная оболочка (см. ). В Р. при очень малых концентрациях растворённого вещества сохраняется структура растворителя. По мере увеличения концентрации возникают новые структуры, например в водных Р. возникают различные структуры .Ионы больших размеров разрушают структуру растворителя, в результате чего появляются экспериментально наблюдаемые неоднородности в этой структуре. Специфическими особенностями характеризуются Р. высокомолекулярных соединений (см. ). Молекулярно-статистическая теория Р. развита лишь для простейших классов Р. Так, при рассмотрении Р. неассоциированных жидкостей часто используют представление о Р. как о статистической совокупности твёрдых образований («сфер», «эллипсоидов», «стержней»), взаимодействующих друг с другом по определённому модельному закону. Для сильно разбавленных Р. электролитов ограничиваются учётом только электростатического взаимодействия ионов как точечных зарядов или как сферических образований определённого радиуса и т.д. Лит.:Кириллин В. А., Шейндлин А. Е., Термодинамика растворов, М., 1956; Шахпаронов М. И., Введение в молекулярную теорию растворов, М., 1956; Prigogine I., The molecular theory of solutions, Arnst., 1957; Робинсон Р., Стокс Р., Растворы электролитов, пер. в англ., М., 1963; Тагер А. А., Физико-химия полимеров, 2 изд., М., 1968; Курс физической химии, под общ. ред. Я. И. Герасимова, 2 изд., т. 1-2, М., 1969-73. Н. Ф. Степанов. «Растдзинад» 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 (
p,
T) +
RTln
x
i, (1)
(
p,
T) +
RTln
x
i, (1)